Elegas en zijn eigenschappen
SF6-gas - elektrisch gas - is zwavelhexafluoride SF6 (zes fluor) ... SF6-gas is de belangrijkste isolator in SF6-geïsoleerde celelementen.
Bij werkdruk en normale temperaturen SF6-gas - kleurloos, reukloos, niet-ontvlambaar gas, 5 keer zwaarder dan lucht (dichtheid 6,7 vs. 1,29 voor lucht), molecuulgewicht ook 5 keer dat van lucht.
SF6-gas veroudert niet, dat wil zeggen, het verandert zijn eigenschappen niet in de loop van de tijd; het ontleedt tijdens een elektrische ontlading, maar recombineert snel en herwint zijn oorspronkelijke diëlektrische sterkte.
 Bij temperaturen tot 1000 K is SF6-gas inert en hittebestendig, tot temperaturen van ongeveer 500 K is het chemisch inactief en niet agressief ten opzichte van de metalen die worden gebruikt bij de constructie van SF6-schakelapparatuur.
Bij temperaturen tot 1000 K is SF6-gas inert en hittebestendig, tot temperaturen van ongeveer 500 K is het chemisch inactief en niet agressief ten opzichte van de metalen die worden gebruikt bij de constructie van SF6-schakelapparatuur.
In een elektrisch veld heeft SF6-gas het vermogen om elektronen op te vangen, wat resulteert in een hoge diëlektrische sterkte van SF6-gas. Door elektronen op te vangen, vormt SF6-gas ionen met een lage mobiliteit die langzaam worden versneld in een elektrisch veld.
Prestaties van SF6-gas verbeteren in een uniform veld, daarom moet het ontwerp van individuele elementen van de schakelapparatuur voor operationele betrouwbaarheid de grootste uniformiteit en homogeniteit van het elektrische veld garanderen.
In een inhomogeen veld treden lokale overspanningen van het elektrische veld op, die corona-ontladingen veroorzaken. Onder invloed van deze lozingen ontleedt SF6, waarbij lagere fluoriden (SF2, SF4) in het milieu worden gevormd, die een schadelijk effect hebben op structurele materialen. compleet gasgeïsoleerd schakelmateriaal (GIS).
Om lekken te voorkomen, zijn alle oppervlakken van individuele elementen van metalen onderdelen en roosters van cellen schoon en glad en mogen ze geen ruwheid en bramen vertonen. De verplichting om aan deze eisen te voldoen wordt gedicteerd door het feit dat vuil, stof, metaaldeeltjes ook lokale spanningen in het elektrische veld veroorzaken en daardoor de diëlektrische sterkte van de SF6-isolatie verslechtert.
Hoge diëlektrische sterkte van SF6-gas maakt het mogelijk om de isolatieafstanden bij lage werkdruk van het gas te verkleinen, waardoor het gewicht en de afmetingen van de elektrische apparatuur worden verminderd. Dit maakt het op zijn beurt mogelijk om de omvang van schakelapparatuur te verkleinen, wat erg belangrijk is, bijvoorbeeld voor de omstandigheden in het noorden, waar elke kubieke meter pand erg duur is.
Hoge diëlektrische sterkte van SF6-gas zorgt voor een hoge mate van isolatie met minimale afmetingen en afstanden, en het goede boogdovende vermogen en koelvermogen van SF6 verhogen het breekvermogen van schakelapparaten en verminderen verhitting van onder spanning staande delen.
Het gebruik van SF6-gas maakt het mogelijk om, onder gelijkblijvende omstandigheden, de huidige belasting met 25% te verhogen en de toegestane temperatuur van koperen contacten tot 90 ° C (in lucht 75 ° C) vanwege chemische weerstand, niet-ontvlambaarheid, brandveiligheid en grotere koelcapaciteit van SF6-gas.
Een nadeel van SF6 is de overgang naar een vloeibare toestand bij relatief hoge temperaturen, wat extra eisen stelt aan het temperatuurregime van de in bedrijf zijnde SF6-apparatuur. De figuur toont de afhankelijkheid van de toestand van SF6-gas van de temperatuur.
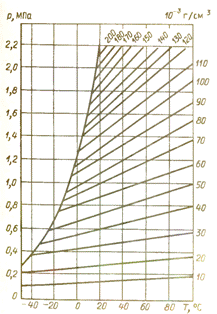
Grafiek van de toestand van SF6-gas versus temperatuur
Voor de werking van SF6-apparatuur bij negatieve temperaturen minus 40 gr.Het is noodzakelijk dat de druk van het SF6-gas in het apparaat niet hoger is dan 0,4 MPa bij een dichtheid van niet meer dan 0,03 g / cm3.
Naarmate de druk toeneemt, zal het SF6-gas vloeibaar worden bij een hogere temperatuur. daarom, om de betrouwbaarheid van elektrische apparatuur bij temperaturen van ongeveer minus 40 ° C te verbeteren, moet deze worden verwarmd (het reservoir van een SF6-stroomonderbreker wordt bijvoorbeeld verwarmd tot plus 12 ° C om te voorkomen dat SF6-gas in een vloeistof terechtkomt staat).
De boogcapaciteit van SF6-gas is, bij gelijkblijvende omstandigheden, vele malen groter dan die van lucht. Dit wordt verklaard door de samenstelling van het plasma en de temperatuurafhankelijkheid van de warmtecapaciteit, warmte en elektrische geleiding.
In de plasmatoestand vallen SF6-moleculen uiteen. Bij temperaturen in de orde van grootte van 2000 K neemt de warmtecapaciteit van SF6-gas sterk toe door de dissociatie van de moleculen. Daarom is de thermische geleidbaarheid van plasma in het temperatuurbereik van 2000 - 3000 K veel hoger (met twee ordes van grootte) dan die van lucht. Bij temperaturen in de orde van 4000 K neemt de dissociatie van moleculen af.
Tegelijkertijd draagt de atomaire zwavel met een laag ionisatiepotentieel gevormd in de SF6-boog bij aan een concentratie van elektronen die voldoende is om de boog te behouden, zelfs bij temperaturen in de orde van grootte van 3000 K. Naarmate de temperatuur verder stijgt, neemt de geleidbaarheid van het plasma af , het bereiken van de thermische geleidbaarheid van lucht en neemt dan weer toe. Dergelijke processen verminderen de spanning en weerstand van een brandende boog in SF6-gas met 20 - 30% in vergelijking met een boog in lucht tot temperaturen in de orde van grootte van 12.000 - 8.000 K. Als gevolg hiervan neemt de elektrische geleidbaarheid van het plasma af.
Bij temperaturen van 6000 K wordt de mate van ionisatie van atomaire zwavel aanzienlijk verminderd en wordt het mechanisme van elektronenvangst door vrij fluor, lagere fluoriden en SF6-moleculen verbeterd.
Bij temperaturen van ongeveer 4000 K eindigt de dissociatie van moleculen en begint de recombinatie van moleculen, de elektronendichtheid neemt nog meer af naarmate atomaire zwavel chemisch combineert met fluor. In dit temperatuurbereik is de thermische geleidbaarheid van het plasma nog steeds aanzienlijk, de boog wordt gekoeld, dit wordt ook vergemakkelijkt door de verwijdering van vrije elektronen uit het plasma vanwege hun invanging door SF6-moleculen en atomair fluor. De diëlektrische sterkte van de opening neemt geleidelijk toe en herstelt zich uiteindelijk.
Een kenmerk van het doven van de boog in SF6-gas ligt in het feit dat bij een stroom die bijna nul is, de dunne boogstaaf nog steeds wordt vastgehouden en afbreekt op het laatste moment van de kruising van de stroom door de nul.Bovendien, nadat de stroom door nul is gegaan, koelt de restboogkolom in het SF6-gas intensief af, onder meer vanwege de nog grotere toename van de warmtecapaciteit van het plasma bij temperaturen in de orde van grootte van 2000 K, en neemt de diëlektrische sterkte snel toe .
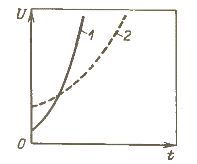
De toename van de diëlektrische sterkte van SF6-gas (1) en lucht (2)
Een dergelijke stabiliteit van boogverbranding in SF6-gas tot minimale stroomwaarden bij relatief lage temperaturen resulteert in de afwezigheid van stroomonderbrekingen en grote overspanningen tijdens het doven van de boog.
In lucht is de diëlektrische sterkte van de opening op het moment dat de boogstroom nul passeert groter, maar vanwege de grote tijdconstante van de boog in lucht is de toenamesnelheid van de diëlektrische sterkte nadat de stroom nul passeert kleiner.

