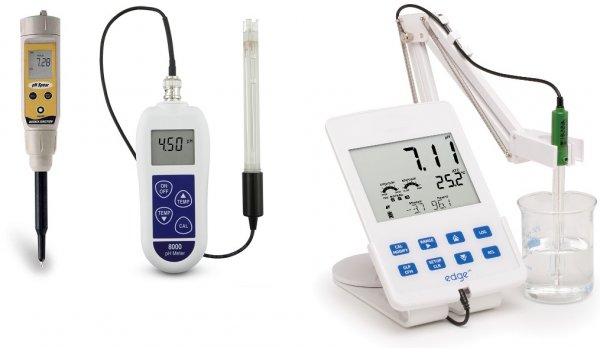
Het principe van pH-meting, apparaat en soorten pH-meters
Om snel de pH-waarde (lees: de zuurgraad) van verschillende media te bepalen, worden pH-meters gebruikt. Industrieel of drinkwater, zuur, zout of alkalische oplossing, bloed, urine en andere lichaamsvloeistoffen, fruit, groenten en andere voedingsmiddelen, medicijnen, enz. — in principe kan alles voorwerp worden van operationeel onderzoek pH-waarde.
Het meten van PH is in wezen een meting van de activiteit van waterstofionen in een medium. En zelfs de aanduiding pH zelf is letterlijk vertaald van het Latijnse "pondus Hydrogenii" als "gewicht van waterstof".
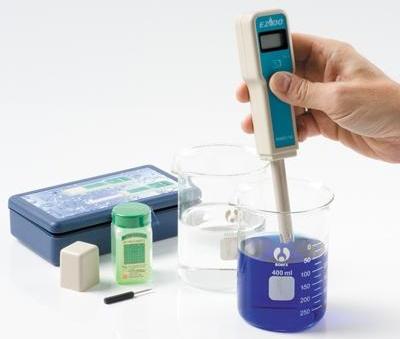
Tegenwoordig worden pH-meters veel gebruikt in de microbiologie en geneeskunde, in waterbehandeling en agrochemie, in bodemkunde, in hydrocultuur, in laboratorium- en veldonderzoek, in de chemische en voedingsindustrie, in de aquaristiek en op veel andere plaatsen.
Met de moderne pH-meter kunt u nauwkeurig en snel de pH-waarde bepalen.Als de pH 7 is, is het medium neutraal, zoals gedestilleerd water, waarin de positieve waterstofionen H+ en de negatieve hydroxide-ionen OH- gelijk verdeeld zijn. Als de zuurgraad hoger is dan 7, is het medium alkalisch. Als de pH lager is dan 7, is het medium zuur.
En hoewel chemici altijd in staat zijn geweest om de zuurgraad van het medium te bepalen volgens de klassieke methode, met behulp van indicatoren, bijvoorbeeld fenolftaleïne, is het bij sommige processen eenvoudigweg nodig om deze indicator nauwkeurig te kwantificeren, en soms is het nodig om constant te controleren het, voor regelen om het te corrigeren. Hiervoor zijn pH-meters uitgevonden.
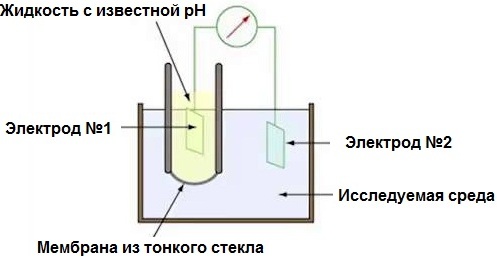
De pH-meter is eigenlijk een elektronische millivoltmeter omdat hij het potentiaalverschil meet tussen het elektrochemische systeem van een paar elektroden en het testmedium waarin ze zijn geplaatst. Het is waar dat de schaal van het apparaat hier niet in millivolt, maar in pH is gegradueerd, aangezien de gemeten EMF evenredig blijkt te zijn met de pH.
Twee elektroden: een glasindicator (oxidatiemiddelen zijn niet bang voor borosilicaatglas) en zilverchloride - een extra referentie-elektrode. De glaselektrode heeft een zeer hoge weerstand van tientallen megohm, en dit is slechts de basisvereiste — de weerstand van de sonde mag niet minder zijn dan 0,1 GΩ. De pH-meter wordt gekalibreerd met behulp van bufferoplossingen met een bekende pH.
Omdat de EMF-waarde wordt beïnvloed door de temperatuur, heeft elk dergelijk meetapparaat een temperatuurcompensatie voor metingen bij andere temperaturen dan + 25 ° C.Maar om een zeer hoge nauwkeurigheid te bereiken, is het noodzakelijk om nauwkeurig te meten bij een temperatuur van +25°C, daarom zijn veel pH-meters uitgerust met een ingebouwde thermometer, zodat je de temperatuur van het medium direct kunt volgen in het proces van onderzoek.
De indicatorglaselektrode in de vorm van een buis met aan het uiteinde een dunwandige kogel, gemaakt van een speciaal elektrisch geleidend borosilicaatglas, is in wezen verbonden met een elektrisch circuit. De beweging van positieve H + -ionen in zo'n glas maakt het mogelijk om het te gebruiken (kationen in het glas bewegen ten opzichte van het polyanion van kiezelzuur). Een suspensie van zilverchloride in een oplossing van zoutzuur wordt in de reageerbuis gegoten, waarna er een zilverdraad in wordt gedompeld - zo wordt een zilverchloride-elektrode verkregen.
De glaselektrode wordt in het testmedium neergelaten, het elektrische circuit wordt gesloten door er een extra referentie-elektrode (kwikcalomelpasta in kaliumchlorideoplossing) in te plaatsen (via een elektrolytische schakelaar of direct). Kaliumchloride zorgt voor contact tussen het kwik-calomelgedeelte van de cel en het testmedium. Deze extra elektrode wordt meestal in een glazen behuizing geplaatst die ondoordringbaar is voor H + ionen.
Het geleidende contact van de kaliumchloride-oplossing in de referentie-elektrode met de testoplossing wordt gevormd door een dunne draad of capillair in een glazen behuizing.Op deze manier wordt een galvanische cel verkregen uit een referentie-elektrode en een zilverchloride-elektrode, en het elektrolytgedeelte van de cel omvat een geleidende glasfilm en een testomgeving.
De EMF van het elektrodesysteem wordt gemeten met een millivoltmeter, de schaal is gegradueerd in pH.Elektronen van de zilverchloride-elektrode worden onder invloed van de gemeten EMF naar de referentie-elektrode overgebracht, wat altijd gepaard gaat met de overdracht van een gelijk aantal protonen van de binnenkant van de glaselektrode naar het medium.
Als we in dit geval de concentratie van positieve waterstofionen H + nemen in de constante van de glaselektrode, dan zal de EMF een functie zijn van de activiteit van H +, dat wil zeggen een functie van de pH van het medium dat wordt bestudeerd.
Moderne modellen pH-meters werken dankzij microprocessors die temperatuurcompensatie uitvoeren en veel gerelateerde taken oplossen. Hoe complexer het apparaat, hoe meer taken het kan oplossen. De nauwkeurigheidsklasse van instrumenten verschilt per model en voor verschillende toepassingen kan een geschikte pH-meter worden gekozen.
Er zijn pH-meters in zakformaat voor huishoudelijk gebruik, er zijn professionele laboratorium-, draagbare en industriële stationaire meters. Sommige pH-meters meten de concentratie van ionen in het medium, het gehalte aan nitraten, enz., hebben een ingebouwd geheugen om de resultaten op te slaan, de mogelijkheid om te communiceren met een computer en de functie van het aanpassen van parameters via een feedbacklus.