Hoe batterijen werken en werken
 In de breedste zin van het woord in technologie verwijst de term "batterij" naar een apparaat dat het mogelijk maakt om onder bepaalde bedrijfsomstandigheden een bepaald type energie te accumuleren en in andere om het te gebruiken voor menselijke behoeften.
In de breedste zin van het woord in technologie verwijst de term "batterij" naar een apparaat dat het mogelijk maakt om onder bepaalde bedrijfsomstandigheden een bepaald type energie te accumuleren en in andere om het te gebruiken voor menselijke behoeften.
Ze worden daar gebruikt waar het nodig is om gedurende een bepaalde tijd energie op te vangen en deze vervolgens te gebruiken om grote arbeidsintensieve processen uit te voeren. Met hydraulische accumulatoren die in sluizen worden gebruikt, kunnen schepen bijvoorbeeld naar een nieuw niveau op de rivierbedding stijgen.
Elektrische batterijen werken met elektriciteit volgens hetzelfde principe: eerst accumuleren (accumuleren) ze elektriciteit van een externe oplaadbron en geven deze vervolgens aan aangesloten verbruikers om werk te doen. Door hun aard behoren ze tot chemische stroombronnen die in staat zijn om periodieke cycli van ontlading en herhaaldelijk opladen uit te voeren.
Tijdens bedrijf vinden er constant chemische reacties plaats tussen de componenten van de elektrodeplaten met hun vulsubstantie - elektrolyt.
Een schematisch diagram van een batterijapparaat kan worden weergegeven door een vereenvoudigde tekening wanneer twee platen van verschillende metalen met draden in het lichaam van het vat worden gestoken om elektrische contacten te verschaffen. Tussen de platen wordt een elektrolyt gegoten.
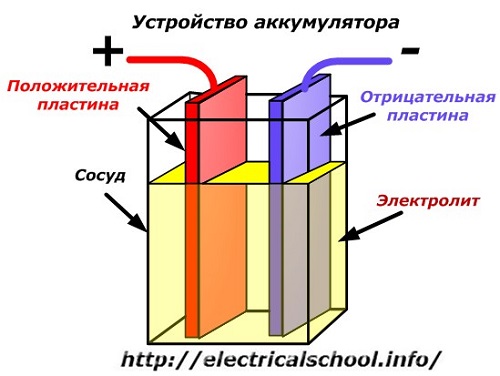
Batterijwerking wanneer ontladen
Wanneer een belasting, zoals een gloeilamp, wordt aangesloten op de elektroden, ontstaat er een gesloten elektrisch circuit waar de ontladingsstroom doorheen vloeit. Het wordt gevormd door de beweging van elektronen in metalen delen en anionen met kationen in de elektrolyt.
Dit proces wordt conventioneel weergegeven in een diagram met een ontwerp van een nikkel-cadmium-elektrode.
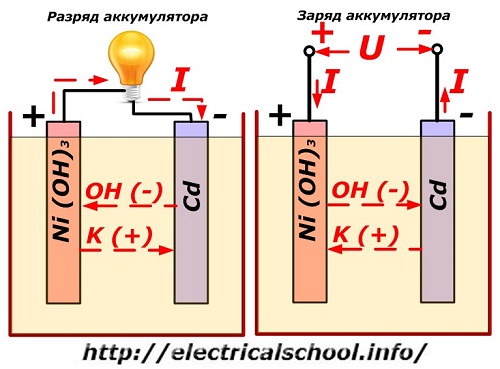
Hier worden nikkeloxiden met grafietadditieven, die de elektrische geleidbaarheid verhogen, gebruikt als het materiaal van de positieve elektrode. Het metaal van de negatieve elektrode is sponzig cadmium.
Tijdens de ontlading komen actieve zuurstofdeeltjes van nikkeloxiden vrij in het elektrolyt en worden ze naar de negatieve platen geleid, waar het cadmium wordt geoxideerd.
Batterijprestaties tijdens het opladen
Wanneer de belasting is uitgeschakeld, wordt een constante (in bepaalde situaties pulserende) spanning aangelegd op de plaataansluitingen met een grotere waarde dan die van een opgeladen batterij met dezelfde polariteit, wanneer de plus- en minaansluitingen van de bron en de consument samenvallen .
De lader heeft altijd meer vermogen, wat de restenergie in de batterij "onderdrukt" en een elektrische stroom creëert in de tegenovergestelde richting van ontlading. Hierdoor veranderen de interne chemische processen tussen de elektroden en de elektrolyt. Op een doos met nikkel-cadmiumplaten is de positieve elektrode bijvoorbeeld verrijkt met zuurstof en de negatieve - tot een staat van puur cadmium.
Wanneer de batterij wordt ontladen en opgeladen, verandert de chemische samenstelling van het materiaal van de platen (elektroden), maar de elektrolyt verandert niet.
Batterij verbindingsmethoden
Parallelle verbinding
De hoeveelheid ontlaadstroom die een persoon kan weerstaan, hangt van veel factoren af, maar vooral van het ontwerp, de gebruikte materialen en hun afmetingen. Hoe groter het oppervlak van de platen bij de elektroden, hoe groter de stroom die ze kunnen weerstaan.
Dit principe wordt gebruikt om cellen van hetzelfde type parallel in batterijen te schakelen wanneer het nodig is om de stroom naar de belasting te verhogen, maar om een dergelijk ontwerp op te laden, zal het vermogen van de bron moeten worden vergroot. Deze methode wordt zelden gebruikt voor kant-en-klare constructies, omdat het nu veel gemakkelijker is om meteen de benodigde batterij aan te schaffen. Maar fabrikanten van zure batterijen gebruiken het door verschillende platen in afzonderlijke blokken te verbinden.
Seriële verbinding
Afhankelijk van de gebruikte materialen kan een spanning van 1,2 / 1,5 of 2,0 volt worden gegenereerd tussen de twee elektrodeplaten van batterijen die in het dagelijks leven gebruikelijk zijn. (Eigenlijk is dit bereik veel groter.) Voor veel elektrische apparaten is dit natuurlijk niet voldoende. Daarom worden batterijen van hetzelfde type in serie geschakeld, en dit gebeurt vaak in één geval.
Een voorbeeld van een dergelijk ontwerp is de wijdverbreide ontwikkeling in de auto-industrie op basis van zwavelzuur en loden elektrodeplaten.
Gewoonlijk is het onder mensen, vooral onder transportchauffeurs, gebruikelijk om elk apparaat een batterij te noemen, ongeacht het aantal samenstellende elementen - dozen. Dit is echter niet helemaal correct.De structuur, samengesteld uit verschillende in serie geschakelde dozen, is al een batterij, waarvoor de afgekorte naam «АКБ» is aangebracht... De interne structuur wordt getoond in de figuur.
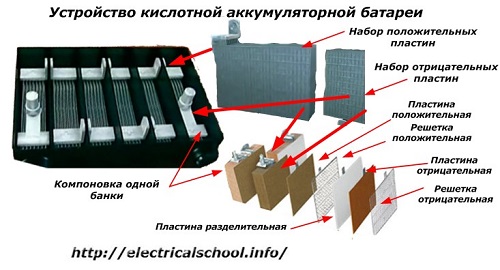
Elk van de potten bestaat uit twee blokken met een set platen voor de positieve en negatieve elektroden. De blokken passen zonder metaalcontact in elkaar met de mogelijkheid van een betrouwbare galvanische verbinding door het elektrolyt.
In dit geval hebben de contactplaten een extra rooster en zijn ze van elkaar gescheiden door een scheidingsplaat.
Door de platen in blokken te verbinden, vergroot u hun werkgebied, vermindert u de totale weerstand van de hele constructie en kunt u het vermogen van de aangesloten belasting vergroten.
Aan de buitenkant van de doos heeft zo'n batterij de elementen die in de onderstaande afbeelding zijn weergegeven.
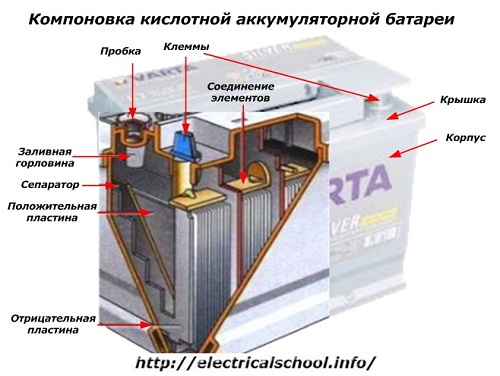
Het laat zien dat de stevige plastic behuizing is afgesloten met een deksel en is uitgerust met twee aansluitingen (meestal kegelvormig) aan de bovenzijde voor aansluiting op het elektrische circuit van de auto. Polariteitsmarkeringen zijn op hun aansluitingen gestempeld: «+» en «-«. Gewoonlijk heeft de positieve pool een iets grotere diameter dan de negatieve pool om bedradingsfouten te voorkomen.
Onderhoudsvriendelijke batterijen hebben een vulopening aan de bovenkant van elke pot om het elektrolytniveau te regelen of gedestilleerd water toe te voegen tijdens gebruik. Er is een plug in geschroefd, die de interne holtes van de behuizing beschermt tegen vervuiling en tegelijkertijd voorkomt dat de elektrolyt morst als de batterij wordt gekanteld.
Omdat bij een krachtige lading gasvorming uit de elektrolyt mogelijk is (en dit proces is mogelijk tijdens intensief rijden), worden gaten in de pluggen gemaakt om te voorkomen dat de druk in de bak toeneemt.Zuurstof en waterstof, evenals elektrolytdampen, gaan er doorheen. Het wordt aanbevolen dergelijke situaties met te hoge laadstromen te vermijden.
Dezelfde figuur toont de verbinding van de elementen tussen de banken en de opstelling van de elektrodeplaten.
Autostartaccu's (loodzuur) werken volgens het principe van dubbele sulfatering. Tijdens het ontladen / opladen vindt er een elektrochemisch proces op plaats, vergezeld van een verandering in de chemische samenstelling van de actieve massa van de elektroden met het vrijkomen / absorberen van water in de elektrolyt (zwavelzuur).
Dit verklaart de toename van het soortelijk gewicht van de elektrolyt bij het opladen en de afname bij het ontladen van de batterij. Met andere woorden, met de dichtheidswaarde kunt u de elektrische toestand van de batterij beoordelen. Om het te meten, wordt een speciaal apparaat gebruikt: een auto-hydrometer.
Gedestilleerd water, dat deel uitmaakt van de elektrolyt van zuuraccu's, verandert in een vaste toestand - ijs bij negatieve temperaturen.Om te voorkomen dat auto-accu's bij koud weer bevriezen, is het daarom noodzakelijk om speciale maatregelen toe te passen waarin de regels voorzien voor uitbuiting.
Welke soorten batterijen zijn er?
Moderne productie voor verschillende doeleinden produceert meer dan drie dozijn producten met verschillende samenstelling van elektroden en elektrolyt. 12 bekende modellen werken alleen op lithium.

Het volgende kan worden gevonden als elektrodemetaal:
-
leiding;
-
ijzer;
-
lithium;
-
titanium;
-
kobalt;
-
cadmium;
-
nikkel;
-
zink;
-
zilver;
-
vanadium;
-
aluminium
-
enkele andere artikelen.
Ze beïnvloeden de elektrische uitgangskarakteristieken en daarmee de toepassing.
Het vermogen om op korte termijn hoge belastingen te weerstaan die het gevolg zijn van de rotatie van de krukassen van verbrandingsmotoren door elektrische startmotoren is kenmerkend voor loodzuuraccu's. Ze worden veel gebruikt in transport, noodstroomvoorzieningen en noodstroomsystemen.
Standaard galvanische cellen (gewone batterijen) worden meestal vervangen door nikkel-cadmium-, nikkel-zink- en nikkel-metaalhydridebatterijen.
Maar lithium-ion- of lithium-polymeerontwerpen werken betrouwbaar in mobiele en computerapparatuur, bouwgereedschap en zelfs elektrische voertuigen.
Afhankelijk van het gebruikte type elektrolyt zijn de batterijen:
-
zuur
-
alkalisch.
Er is een classificatie van batterijen volgens doel. In moderne omstandigheden zijn er bijvoorbeeld apparaten verschenen die worden gebruikt voor energieoverdracht - het opladen van andere bronnen. De zogenaamde externe batterij helpt de eigenaren van veel mobiele apparaten bij het ontbreken van een wisselend elektrisch netwerk. Het is in staat om herhaaldelijk een tablet, smartphone of mobiele telefoon op te laden.
Al deze batterijen hebben hetzelfde werkingsprincipe en een soortgelijk apparaat. Het lithium-ionvingermodel dat in de onderstaande afbeelding wordt weergegeven, herhaalt bijvoorbeeld in veel opzichten het ontwerp van de eerder besproken zuurbatterijen.
Hier zien we dezelfde contactelektroden, platen, separator en behuizing. Alleen ze zijn gemaakt rekening houdend met andere arbeidsomstandigheden.
Elektrische basiskenmerken van een batterij
De werking van het apparaat wordt beïnvloed door de parameters:
-
capaciteit;
-
energiedichtheid;
-
zelfontlading;
-
temperatuurregime.
Capaciteit wordt de maximale lading van de batterij genoemd, die deze kan geven tijdens het ontladen tot de laagste spanning. Het wordt uitgedrukt in hangers (SI-systeem) en ampère-uren (niet-systeemeenheid).
Als soort capaciteit is er «energiecapaciteit», die de energie bepaalt die vrijkomt tijdens het ontladen tot de minimaal toegestane spanning. Het wordt gemeten in joules (SI) en wattuur (niet-SI-eenheden).
Energiedichtheid uitgedrukt als de verhouding van de hoeveelheid energie tot het gewicht of volume van de batterij.
Zelfontlading houdt rekening met capaciteitsverlies na opladen bij afwezigheid van belasting van de klemmen. Dit hangt af van het ontwerp en wordt om vele redenen verergerd door isolatiestoringen tussen de elektroden.
De bedrijfstemperatuur beïnvloedt de elektrische eigenschappen en kan bij ernstige afwijkingen van de door de fabrikant opgegeven norm de batterij beschadigen. Hitte en kou zijn onaanvaardbaar, ze beïnvloeden het verloop van chemische reacties en de druk van de omgeving in de doos.
