Waarom diëlektrica geen stroom geleiden
Om de vraag te beantwoorden «waarom geleidt een diëlektricum geen elektriciteit?» over het verschijnen en bestaan van elektrische stroom… En laten we dan vergelijken hoe geleiders en diëlektrica zich gedragen om een antwoord op deze vraag te vinden.
Huidig
Elektrische stroom wordt geordende, dat wil zeggen gerichte beweging van geladen deeltjes genoemd elektrisch veld… Dus, ten eerste, het bestaan van een elektrische stroom vereist de aanwezigheid van gratis geladen deeltjes die in staat zijn om op een gerichte manier te bewegen. Ten tweede is er een elektrisch veld nodig om deze ladingen aan te drijven. En er moet natuurlijk een bepaalde ruimte zijn waarin deze beweging van geladen deeltjes, elektrische stroom genaamd, plaatsvindt.
Gratis geladen deeltjes zijn overvloedig aanwezig in geleiders: in metalen, in elektrolyten, in plasma. In een koperen geleider zijn dit bijvoorbeeld vrije elektronen, in een elektrolyt - ionen, bijvoorbeeld zwavelzuurionen (waterstof en zwaveloxide) in een loodzuuraccu, in plasma - ionen en elektronen zijn het degenen die bewegen tijdens een elektrische ontlading in een geïoniseerd gas.
Metaal
Laten we bijvoorbeeld twee stukken koperdraad nemen en die gebruiken om een kleine gloeilamp op een batterij aan te sluiten. Wat zal er gebeuren? Het licht gaat gloeien, wat betekent dat a gelijkstroom… Tussen de uiteinden van de draden is er nu een potentiaalverschil gecreëerd door de batterij, wat betekent dat er een elektrisch veld in de draad is gaan werken.
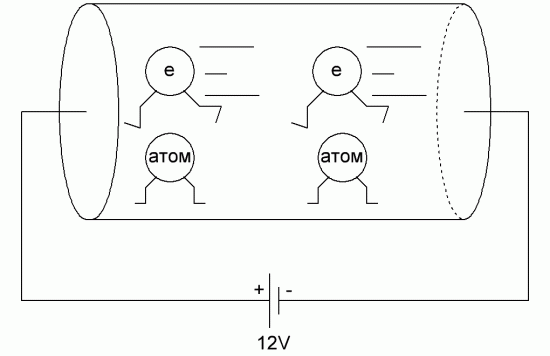
Het elektrische veld dwingt de elektronen van de buitenste schillen van koperatomen om in de richting van het veld te bewegen - van atoom naar atoom, van atoom naar het volgende atoom, enzovoort langs de keten, omdat de elektronen van de buitenste schillen van metaal atomen zijn veel minder sterk gebonden aan kernen dan elektronen dichter bij de kernen van elektronenbanen. Van waar het elektron was achtergelaten, komt een ander elektron uit de negatieve pool van de batterij, dat wil zeggen, elektronen bewegen vrij langs de metalen ketting, waardoor ze gemakkelijk van atomen veranderen.
Ze lijken zich langs het kristalrooster van het metaal te vormen in de richting waarin ze worden geduwd, in een poging het elektrische veld te versnellen (van de min naar de plus van de constante EMF-bron), terwijl de elektronen zich vastklampen aan de atomen van het kristalrooster langs hun hele pad.
Sommige elektronen breken tijdens hun beweging in atomen (vanwege het feit dat de thermische beweging de hele structuur van atomen samen met de elektronen trilt), waardoor de geleider opwarmt - zo manifesteert het zich elektrische weerstand van de draden.
Vrije elektronen in een metaal
De studie van metalen met behulp van röntgenstralen, evenals andere methoden, heeft aangetoond dat metalen een kristallijne structuur hebben.Dit betekent dat ze bestaan uit atomen of moleculen die op een bepaalde manier in de ruimte zijn gerangschikt (in volgorde, ionen) die in alle drie de dimensies de juiste afwisseling creëren.
Onder deze omstandigheden bevinden de atomen van de elementen zich zo dicht bij elkaar dat hun buitenste elektronen in dezelfde mate tot dit atoom behoren als tot de naburige, waardoor de bindingsgraad van het elektron aan elk afzonderlijk atoom is praktisch afwezig.
Afhankelijk van het type metaal is ten minste één van de elektronen van elk atoom, soms twee elektronen en in sommige gevallen zelfs drie elektronen vrij in hun bewegingen in het metaal, onder invloed van van buitenaf opgelegde krachten.

Diëlektrisch
Wat zit er in een diëlektricum? Als je in plaats van koperdraden plastic, papier of iets dergelijks neemt? Er zal geen elektriciteit zijn, er zal geen licht branden. Waarom? De structuur van het diëlektricum is zodanig dat het bestaat uit neutrale moleculen die, zelfs onder invloed van een elektrisch veld, hun elektronen niet in een geordende beweging vrijgeven - dat kunnen ze eenvoudigweg niet. Er zijn geen vrije geleidingselektronen in een diëlektricum, zoals in een metaal.
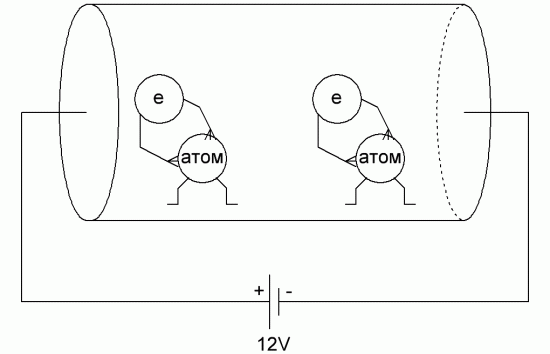
De buitenste elektronen in het atoom van elk diëlektrisch molecuul zijn stevig opeengepakt, bovendien nemen ze deel aan de interne bindingen van het molecuul, terwijl de moleculen van zo'n stof meestal elektrisch neutraal zijn. Het enige dat diëlektrische moleculen kunnen doen, is polariseren.
Onder invloed van een elektrisch veld dat erop wordt toegepast, zullen de bijbehorende elektrische ladingen van elk molecuul eenvoudig iets verschuiven van de evenwichtspositie, terwijl elk geladen deeltje in zijn eigen atoom zal blijven. Dit fenomeen wordt ladingsverplaatsing genoemd diëlektrische polarisatie.
Als gevolg van polarisatie verschijnen er ladingen op het oppervlak van een diëlektricum dat op deze manier is gepolariseerd door een elektrisch veld dat erop wordt aangelegd en die de neiging hebben om het externe elektrische veld dat de polarisatie veroorzaakte met hun elektrische veld te verminderen. Het vermogen van een diëlektricum om op deze manier een extern elektrisch veld te verzwakken wordt genoemd diëlektrische constante.